وهو ناتج عن التحول في كثافة الإلكترون في سحابة الإلكترون، وهي إحدى خصائص الذرة، وهي من أحدث الاكتشافات في الفيزياء.، كأصغر جزء من عنصر كيميائي.
جدول المحتويات
تعريف الإلكترون

قبل أن تحدد الخاصية التي تنتج عن التحول في كثافة الإلكترون في سحابة الإلكترون من الضروري البدء بتعريف الإلكترون أو “الإلكترون” بالإنجليزية، وهو أحد مكونات الذرة ويتميز بشحنته السالبة ووجوده بالقرب من النواة، لأنه يختلف عن باقي الأجزاء المكونة للذرة، سواء كانت بروتونات أو نيوترونات، بكتلتها الصغيرة، وعلى الرغم من توقع العديد من العلماء لوجودها، يعود الفضل في اكتشافها الرسمي إلى العالم البريطاني طومسون في عام 1897، وتجدر الإشارة إلى أن الإلكترونات هي سر توصيل الطاقة الكهربائية في المواد الصلبة.[1]
ينشأ من التحول في كثافة الإلكترون في سحابة الإلكترون
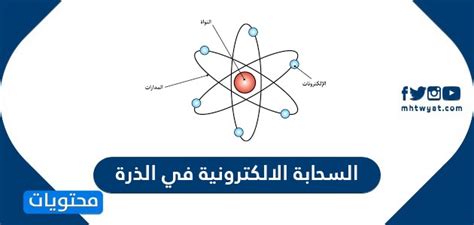
عندما يتم إزاحة كثافة الإلكترون أو نقلها داخل سحابة الإلكترون، يتم إنشاء تجاذب بين العناصر الكيميائية فضاء سالب الشحنة يحمل طاقة معينة، وهو مفهوم يتعلق بالمدار الذري وهو في الواقع وظيفة رياضية تصف حركة الإلكترونات في الذرة.[2]أنا[3]
حركة الإلكترونات حول النواة

من خلال تعريف الإلكترون أعلاه، نستنتج أن الإلكترون يدور حول النواة بسبب جاذبية الجسيمات التي تتكون منها النواة، والعكس بالعكس من حيث الشحنة، مما يسمح بتوزيع الإلكترونات في مدارات حول النواة، مما يسمح يتم تثبيتها على مسافة معينة. من هذا الحدوث تشكل هذه الإلكترونات سحابة سالبة الشحنة، وتجدر الإشارة إلى أن هذا التوزيع الإلكتروني لكل ذرة يحدد حجم الذرة وخصائصها الكيميائية بحيث يمكن تصنيفها إلى باقي العناصر الكيميائية في الجدول الدوري. من العناصر.[3]
اقرأ أيضًا الجسيمات المحايدة في القلب
عدد الإلكترونات في المدار

بعد تحديد الخاصية التي تنتج عن التحول في كثافة الإلكترون في سحابة الإلكترون، تجدر الإشارة إلى أن توزيع الإلكترونات على مستوى كل ذرة على مستوى مدارات متعددة يرجع إلى حجم الفراغ والسحابة في تقع الإلكترونات، ويتمدد كل مدار داخل أربعة مدارات رئيسية مختلفة لإلكترونين ويرمز إلى هذه المدارات مكتوبة بأحرف لاتينية “s، p، f، d”، ويحتوي كل مدار رئيسي على مستويات ثانوية يمكنها تحتوي على أكثر من إلكترونين تآكل.[4]
يخلق التحول في كثافة الإلكترون في سحابة الإلكترون قوة جذب، وهي خاصية تتطلب ة المفاهيم الأساسية للفيزياء، حيث تتكون كل ذرة من البروتونات والنيوترونات والإلكترونات، وكل إلكترون يحمل شحنة سالبة وهو موزعة على مستوى مدارات مختلفة، ولكل عنصر كيميائي خواص فيزيائية ويتم تعريفه كيميائيًا بشكل أساسي في الجدول الدوري للعناصر.
- ^ wikiwand.com، إلكترون، 09/01/2024
- ^ wikiwand.com، كثافة الإلكترونات، 09/01/2024
- ^ Thoughtco.com، تعريف السحب الإلكترونية، 09/01/2024
- ^ toppr.com، كيف يتم توزيع الإلكترونات في مدارات مختلفة (قذائف)، 09/01/2024